ただし、ビウレット反応という名前だが、ビウレットは生成しない。 脚注 ^ Ferdinand Rose (13) "Über die Verbindungen des Eiweiss mit Metalloxyden" (金属酸化物を含む アルブミン 化合物), Poggendorfs Annalen der Physik und Chemie , vol 104, pages , doi /andpビウレット反応 タンパク質およびペプチド (トリペプチド以上) の呈色反応の 1 つ。タンパク質およびペプチドの水酸化アルカリ溶液に希硫酸銅 (ii) 水溶液を数滴加 えると,青紫~赤紫色を呈する。この反応は,ポリペプチド鎖の隣接する 2 残基のこの反応は指紋の検出などに用いられている。 ビウレット反応 ペプチド結合を2つ以上もつペプチドに水酸化ナトリウム水溶液、硫酸銅(Ⅱ)水溶液を順に加えると赤紫色になる。 この反応を ビウレット反応 という。
トップレート ビウレット反応 原理 人気のある画像を投稿する
ビウレット反応 原理 化学式
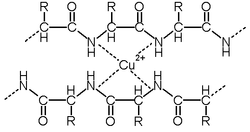
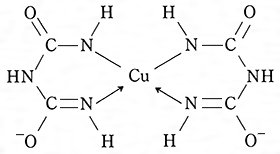
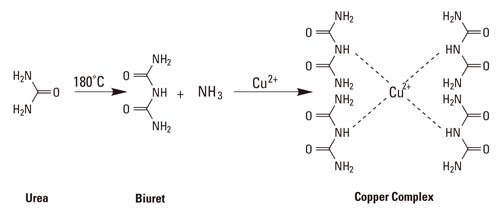
ビウレット反応 原理 化学式-ビウレット biuret NH 2 CONHCONH 2 がこの反応を示す 1個の窒素原子を隔てて存在する2個の-CO-NH-基がCu 2+ に配位 → 銅錯イオン 赤紫色 → ビウレット反応 トリペプチド以上のペプチド → 2つ以上のペプチド結合 手に濃硝酸をつけたことがありませんか測定原理 1.測定原理 検体中の蛋白質はビウレット試薬と反応し赤紫色の錯体 となります。この赤紫色の吸光度を測定することにより 総蛋白量を求めます。 ビウレット試薬 検体中の蛋白質 ─────── 錯体(赤紫色) 2.特長


ビウレット反応とは コトバンク
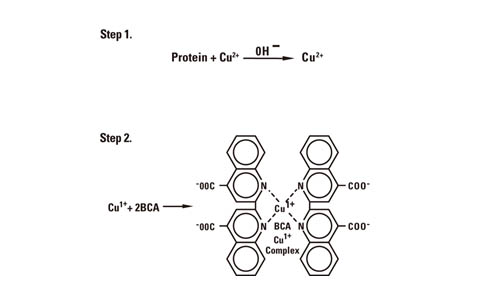
図6 ビウレット法における発色の原理 発色はR1からR4の構造の影響を受けない ビウレット法は、 05 から 5 mg/ml 程度のタンパク質濃度を測定するのに適しているが、より希薄なタンパク質溶液の濃度測定には、 Lowry 法が用いられる。高校化学アミノ酸 5つの検出反応 別府市学習塾 進学予備校ウインロード 上野丘・舞鶴・鶴見丘受験、難関大学受験 中学受験 高校受験 大学受験 医学部受験|数学 物理 化学 英語 に強い塾。小学生・中学生は全教科個別演習指導。ビウレット反応とは、アルカリ性条件下で 3つ以上のアミノ酸からなるペプチド (あるいはタンパク質)が 二価の銅イオン ( Cu(Ⅱ) )と錯体(キレート)を形成することによって、二価の銅イオン(Cu2+)が 一価の銅イオン ( Cu(Ⅰ) )へと還元され、溶液
ビウレット反応を利用してタンパク質を定量することをビウレット法といい、吸光度測定には 波長545 nmの光が用いられます。ビウレット法では5~160 mg/mLの範囲のタンパク質が定量できます。 ローリー法ビウレット反応の溶液は、以下のような紫色を呈する (3)。 広告 ビウレット法の長所と短所 ビウレット法には、以下のような特徴がある (2)。 長所 ペプチド結合を検出するため、アミノ酸組成に影響を受けない。 短所④ビウレット反応 最後に一番厄介な検出反応である「ビウレット反応」です。 ビウレット反応では「2つ以上のペプチド結合」、 つまりトリペプチド以上を検出して、 赤紫色を呈色します。。 なぜこんなに中途半端な数なのかを確認しましょう。
原理:タンパク質をアルカリ性条件下でCu2溶液と反応させ ると、赤紫色を呈する。これはアルカリ条件下でCu2 がポリペプチド鎖中の窒素原子と錯体を形成すること で発色する、いわゆるBiuret反応を利用したものである。④ビウレット反応 最後に一番厄介な検出反応である「ビウレット反応」です。 ビウレット反応では「2つ以上のペプチド結合」、 つまりトリペプチド以上を検出して、 赤紫色を呈色します。。 なぜこんなに中途半端な数なのかを確認しましょう。タンパク質の定量法(BCA法、Bradford法、Lowry法) タンパク質の濃度測定の方法には、 BCA法 、 Bradford法(ブラッドフォード法) 、 Lowry法(ローリー法) などがあります。 BCA法やLowry法の原理を理解するために、まず ビウレット反応 について理解していることが望まれます。


高等学校化学ii 糖類とタンパク質 Wikibooks



トップレート ビウレット反応 原理 人気のある画像を投稿する
図6 ビウレット法における発色の原理 発色はR1からR4の構造の影響を受けない ビウレット法は、 05 から 5 mg/ml 程度のタンパク質濃度を測定するのに適しているが、より希薄なタンパク質溶液の濃度測定には、 Lowry 法が用いられる。〘名〙 (ビウレットはbiuret) 蛋白質の呈色反応の一つ。 試料に水酸化ナトリウム水溶液と硫酸銅溶液を加えると青紫から赤紫色になるもの。 アミノ酸三個以上のペプチドの検出に使われる。BCA法、Bradford法、Lowry法など、"総"タンパク質定量法の原理まとめ|知っておきたい! タンパク質実験あれこれ 第4回 作成者 LATB Staff 0304 第4回目の今回は、 前回 に引きつづき「総タンパク質定量法」をテーマとして、弊社の総タンパク質定量試薬



トップレート ビウレット反応 原理 人気のある画像を投稿する



食品学実験15 カテゴリーの記事一覧 栄養士のための食品学実験
ビウレット法 原理の概略 アルカリ性の条件下で銅イオン (Cu2) をタンパク質溶液と反応させると、Cu1となってこれがペプチド結合と赤紫色の複合体を形成するので、これを分光光度計で測定するという方法がBiuret (ビウレット)法です。 タンパク質の種類による発色の違いが小さく、界面活性また、大まかな反応原理については電気陰性度や有機化学反応(応用)の知識を使うので以下の記事を先にご覧下さい。 電気陰性度と電子親和力、イオン化エネルギーの違い 有機化学反応の仕組み 1ビウレット反応 目的化合物がトリ(3)ペプチド以上かビウレット反応 タンパク質の水溶液に 水酸化ナトリウム水溶液 を加え、 硫酸銅(Ⅱ) 水溶液を少量加えると赤紫色に呈色します。 この反応はタンパク質に2個以上の連続するペプチド結合がある場合に起こる反応で ビウレット反応 といいます。 2個以上並ぶペプチド結合が銅イオン(\(\mathrm



タンパク質の性質について Clear


a法 Bradford法 Lowry法など 総 タンパク質定量法の原理まとめ 知っておきたい タンパク質実験あれこれ 第4回 Learning At The Bench
ビウレット反応 ビウレット反応陽性の必要条件は,隣り合った2 つのペプチド結合が存在することである。 したがって,遊離アミノ酸やジペプチドはビウレット反応陰性である。 反応の原理ビウレット反応の溶液は、以下のような紫色を呈する (3)。 広告 ビウレット法の長所と短所 ビウレット法には、以下のような特徴がある (2)。 長所 ペプチド結合を検出するため、アミノ酸組成に影響を受けない。 短所21反応原理 ニッケル(ii)とビウレットとの錯体の構造は cuビウレット錯体3)のそれと同様で,k2〔ni (nhconhconh)2〕 ・4hで あると報告されて いる4)。したがって,ni一 ビウレット反応により 蛋白質も類似反応が起こり,ペ プチド結合中の 4個 の窒素原子とni2と が


化学


アミノ酸の性質 検出反応まとめ 高校化学 受験メモ
ビウレット反応 Wikipedia ビウレット反応ビウレットはんのうとは コトバンク アミノ酸タンパク質検出反応を総まとめビウレットキ 総タンパク質の定量法 タンパク質やアミノ酸の呈色反応のメカニズムは a法bradford法lowry法など総タンパク質定量法の原理



トップレート ビウレット反応 原理 人気のある画像を投稿する



蛋白質のビウレット反応 検査と技術 7巻2号 医書 Jp



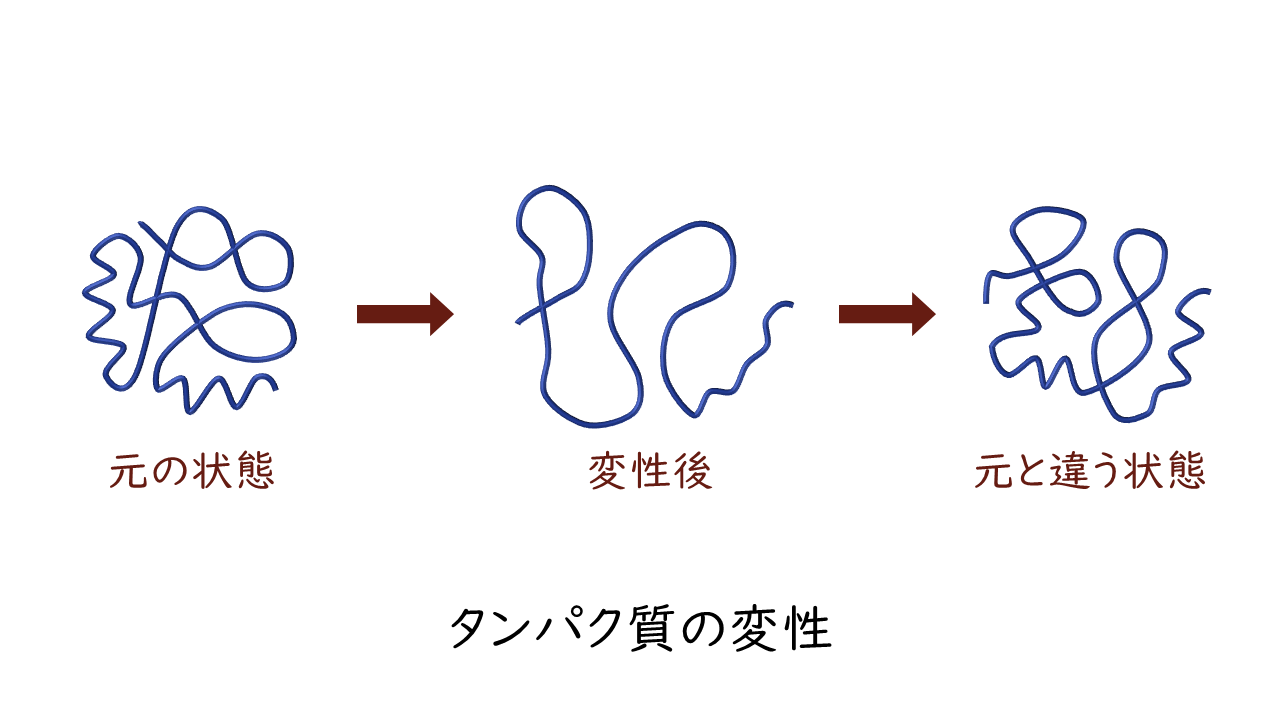
タンパク質の変性といろいろな検出反応



化学 ビウレット反応を3分で覚える動画 Youtube



解決 タンパク質の定量法 a法 Bradford法 Lowry法 の原理と特徴


a法 Bradford法 Lowry法など 総 タンパク質定量法の原理まとめ 知っておきたい タンパク質実験あれこれ 第4回 Learning At The Bench



ビウレット反応とニンヒドリン反応の覚え方 語呂合わせ アミノ酸とタンパク質の検出法 呈色反応 19信州大第4問より 天然高分子 ゴロ化学 Youtube


この間 タンパク質の定性反応の実験をしたため 課題でレポート Yahoo 知恵袋



トップレート ビウレット反応 原理 人気のある画像を投稿する


タンパク質の性質 気になる遺伝子


アミノ酸の性質 検出反応まとめ 高校化学 受験メモ
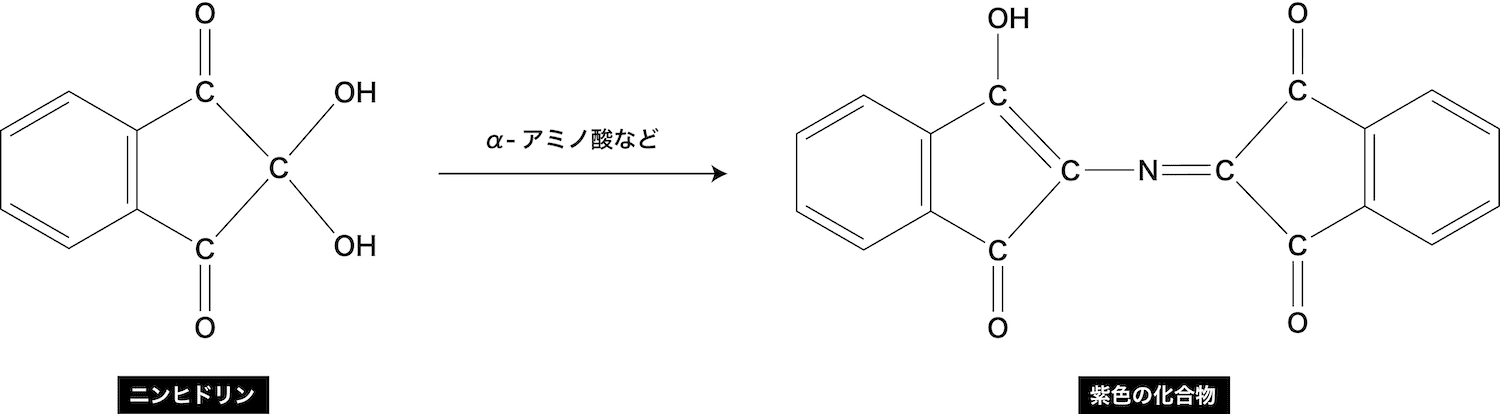


アミノ酸 タンパク質 検出反応を総まとめ ビウレット キサントプロテイン ニンヒドリン 硫黄 化学のグルメ


ビウレット反応なんですが どのような仕組みでトリペプチド以上 Yahoo 知恵袋


第127章 タンパク質の性質



ビウレット反応とは コトバンク



3 1 2 タンパク質
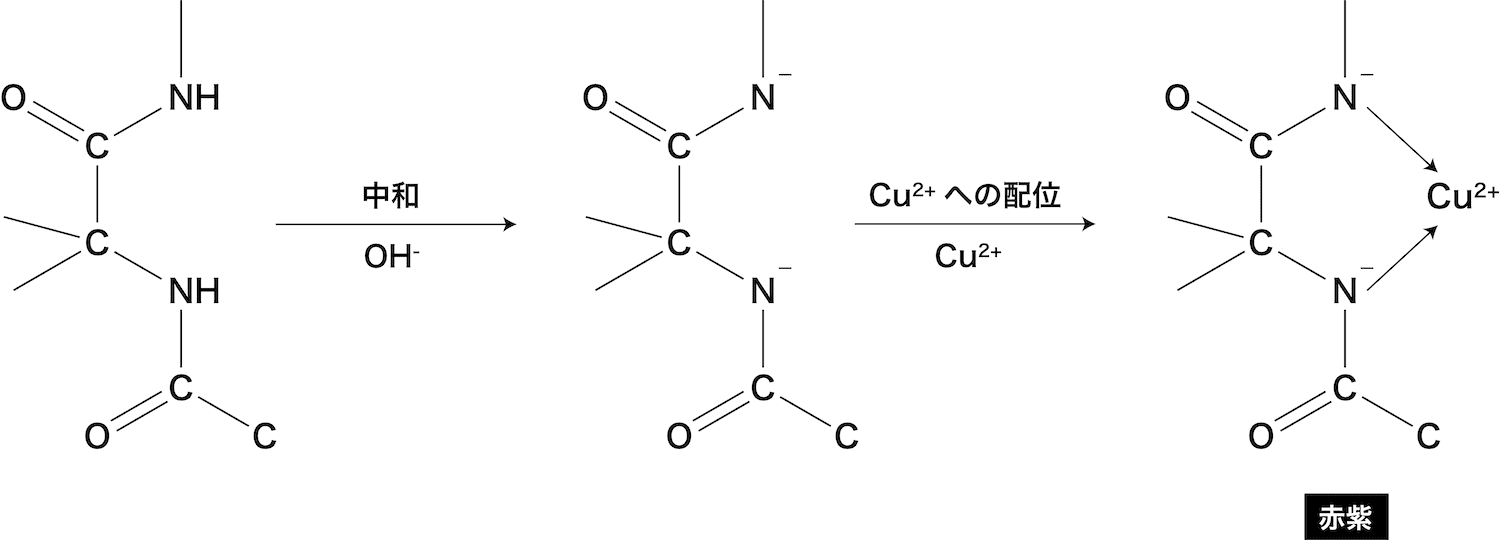


アミノ酸 タンパク質 検出反応を総まとめ ビウレット キサントプロテイン ニンヒドリン 硫黄 化学のグルメ


化学実験 ビウレット反応を見よう 牛乳や卵の白身などで実験 やさしい基礎化学


アミノ酸の性質 検出反応まとめ 高校化学 受験メモ



ビウレット Wikipedia



アミノ酸 タンパク質の検出反応を語呂による覚え方 化学受験テクニック塾



ビウレット Wikipedia



アミノ酸 タンパク質の検出反応を語呂による覚え方 化学受験テクニック塾
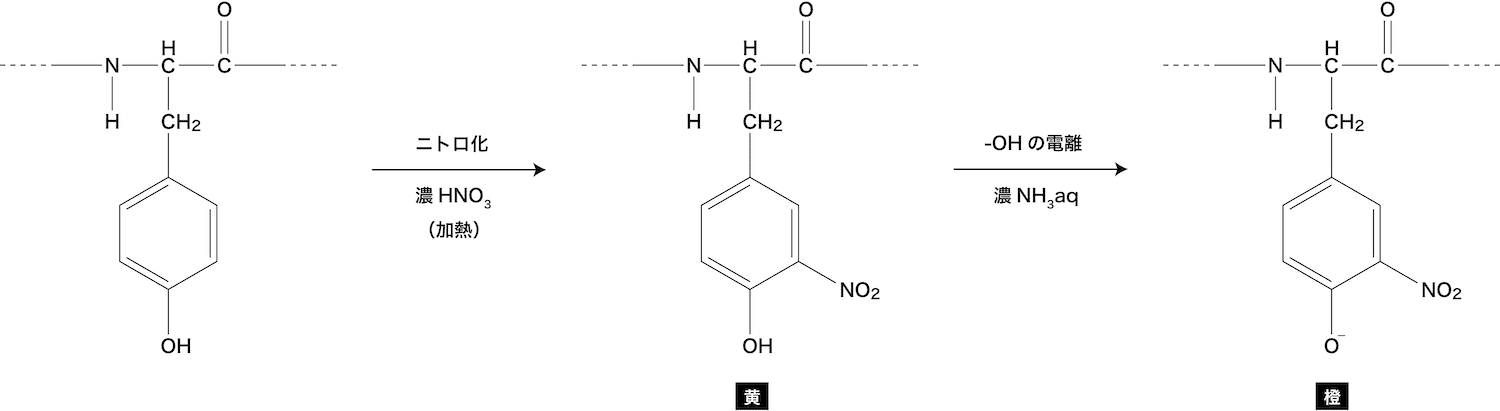


アミノ酸 タンパク質 検出反応を総まとめ ビウレット キサントプロテイン ニンヒドリン 硫黄 化学のグルメ


天然高分子化合物 タンパク質と核酸


アミノ酸のビウレット反応について質問です グリシン チロシン Yahoo 知恵袋
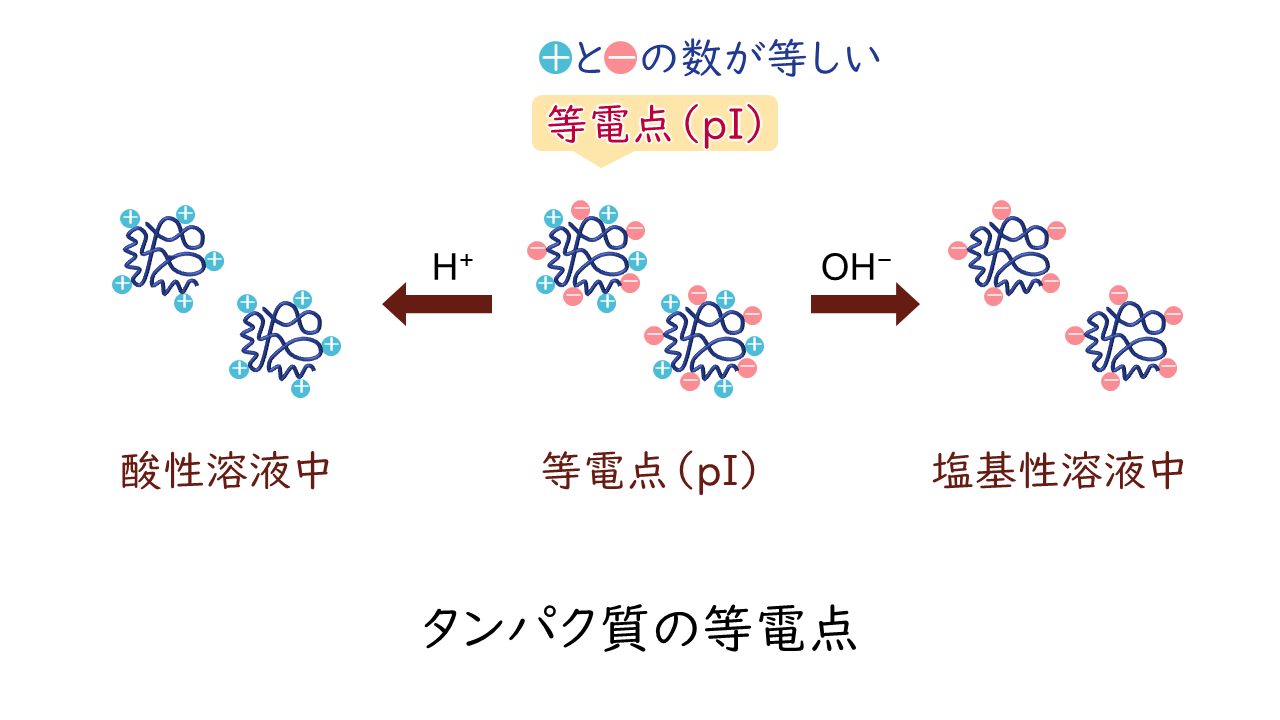


タンパク質の性質 気になる遺伝子



アミノ酸の呈色反応 笑 沈め 団亀供の鬱寥はむぅんらいとの湿原に


第127章 タンパク質の性質


Faq Main


アミノ酸の性質 検出反応まとめ 高校化学 受験メモ


天然高分子化合物 タンパク質と核酸



キサントプロテイン反応 Wikipedia



トップレート ビウレット反応 原理 人気のある画像を投稿する


天然高分子化合物 タンパク質と核酸


名前 裕海 日時 09年06月16日 16時59分28秒 学校で今 化学実験のタンパク質やアミノ酸の定性反応について習っていて どうして青紫色やダイダイ色や黒色に変化するかわかりません 教えてください 名前 芦田 実 日時 09年06月24日 23時



トップレート ビウレット反応 原理 人気のある画像を投稿する



高等学校化学ii 糖類とタンパク質 Wikibooks


たかなっちの高校生物



アミノ酸 タンパク質の検出反応を語呂による覚え方 化学受験テクニック塾



高校化学 高分子化合物 テスト5 第1問 問題編 映像授業のtry It トライイット


4 1 1 アミノ酸とタンパク質


天然高分子化合物 タンパク質と核酸


Chemicalcat Chemicalcatを化学的にあらわすと ビウレット反応 です わからなかったら調べてみよう Bakegaku T Co Jadm5mvp6v ビウレット反応 とは タンパク質が塩基水溶液中でcu とキレート錯体を形成し紫色の呈色を示す反応です キレート


天然高分子化合物 タンパク質と核酸


牛乳からの栄養素の分離と定性反応 実験振り返り 栄養士のための食品学実験


タンパク質の検出方法 ビウレット反応 の質問です ビウレット Yahoo 知恵袋



食品学実験2 管1 タンパク質の定性実験1 Post Test実施 ブログ De 授業 21


アミノ酸の性質 検出反応まとめ 高校化学 受験メモ
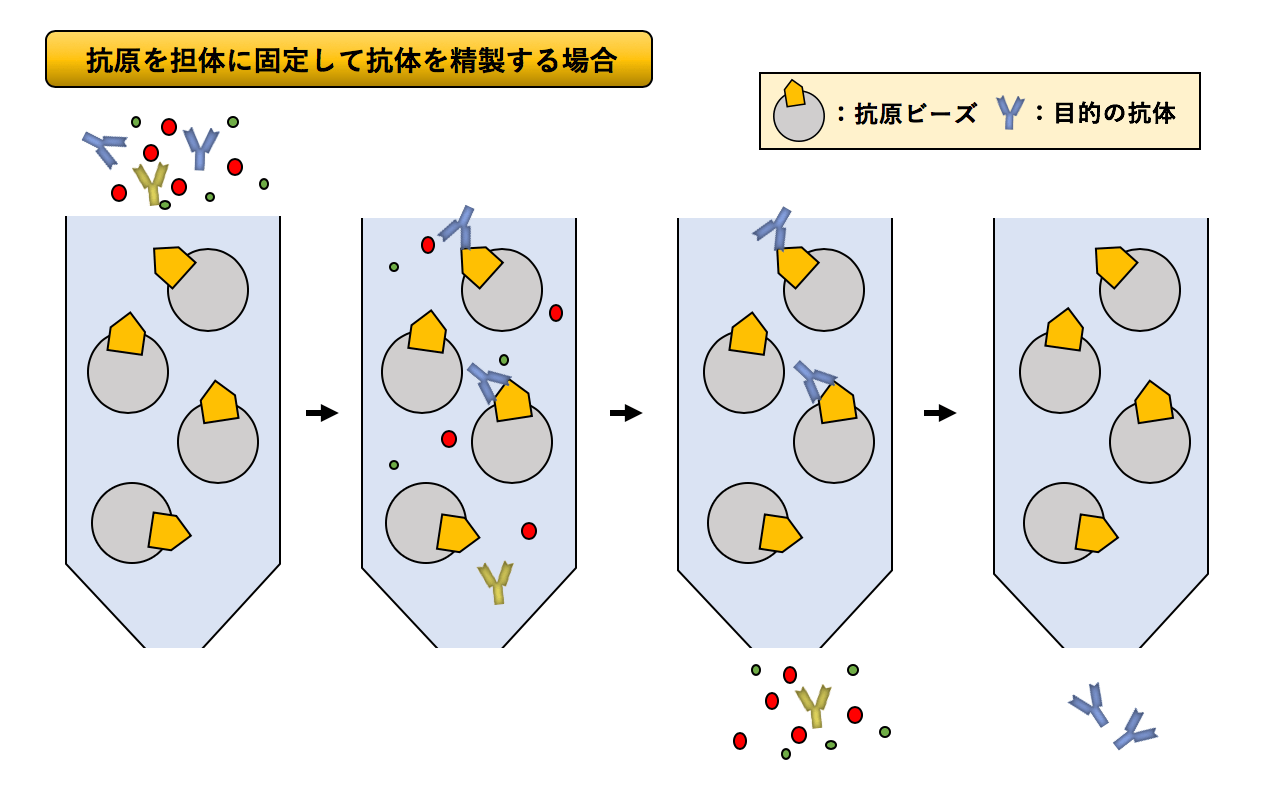


解決 タンパク質の定量法 a法 Bradford法 Lowry法 の原理と特徴


アミノ酸の性質 検出反応まとめ 高校化学 受験メモ



ニンヒドリン反応の利用法と反応機構



3 1 2 タンパク質



高校化学 タンパク質の反応 映像授業のtry It トライイット



タンパク質アミノ酸の呈色反応


天然高分子化合物 タンパク質と核酸
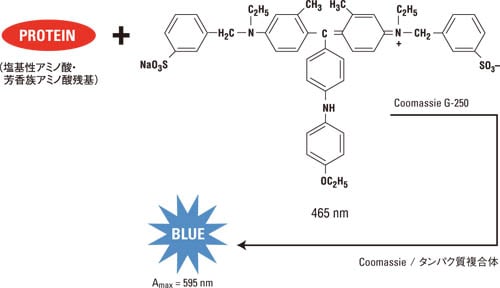


a法 Bradford法 Lowry法など 総 タンパク質定量法の原理まとめ 知っておきたい タンパク質実験あれこれ 第4回 Learning At The Bench


天然高分子化合物 タンパク質と核酸


第126章 実験 タンパク質



ビウレット Biuret Japaneseclass Jp



3 1 2 タンパク質



タンパク質 ペプチドの検出反応4選 仕組み理解で2度と忘れない方法


アミノ酸の性質 検出反応まとめ 高校化学 受験メモ



タンパク質のビウレット反応をわかりやすく簡単に教えてください Clear
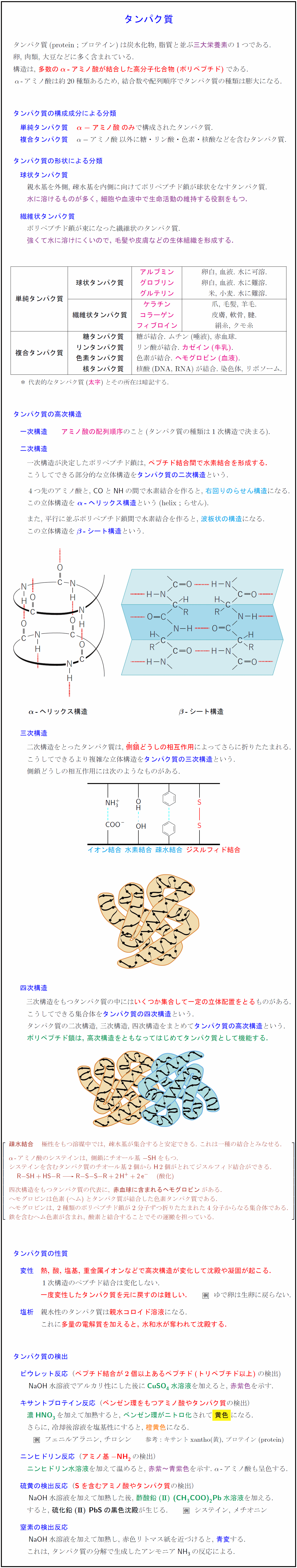


高校高分子化合物 タンパク質の分類 高次構造 一次 四次 性質 検出 受験の月



トップレート ビウレット反応 原理 人気のある画像を投稿する
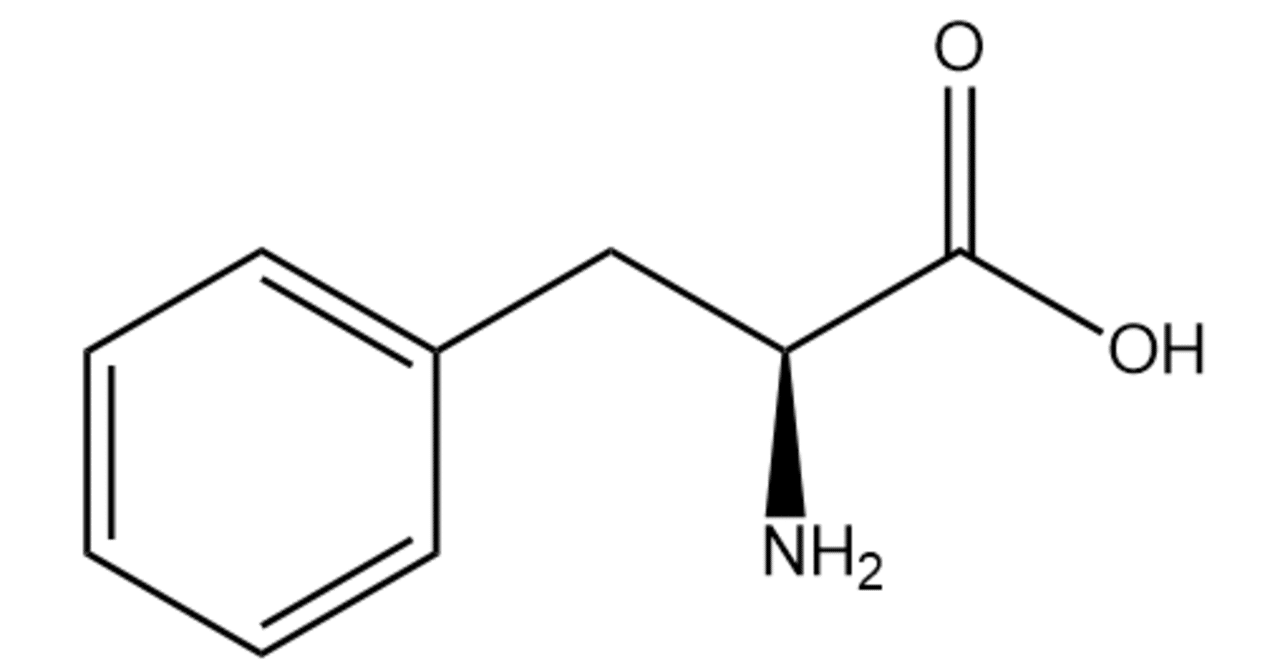


語源で覚える タンパク質の検出反応 化合物語源たん Note



高校化学 タンパク質の反応 映像授業のtry It トライイット


牛乳からの栄養素の分離と定性反応 実験振り返り 栄養士のための食品学実験


トップレート ビウレット反応 原理 人気のある画像を投稿する



ビウレット反応 ビウレット反応の概要 Weblio辞書
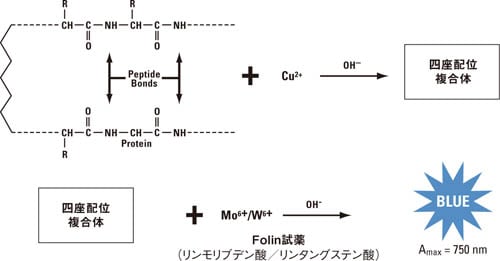


a法 Bradford法 Lowry法など 総 タンパク質定量法の原理まとめ 知っておきたい タンパク質実験あれこれ 第4回 Learning At The Bench



Images Of ビウレット Japaneseclass Jp
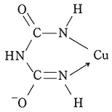


ビウレット反応とは コトバンク
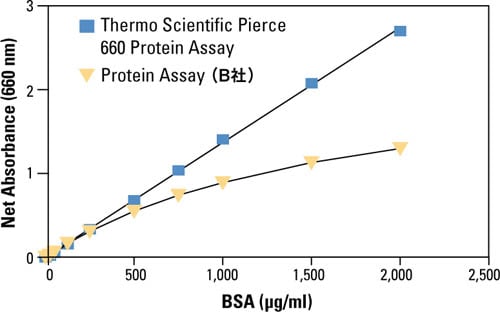


a法 Bradford法 Lowry法など 総 タンパク質定量法の原理まとめ 知っておきたい タンパク質実験あれこれ 第4回 Learning At The Bench



食品学実験2 管1 タンパク質の定性実験1 Post Test実施 ブログ De 授業 21
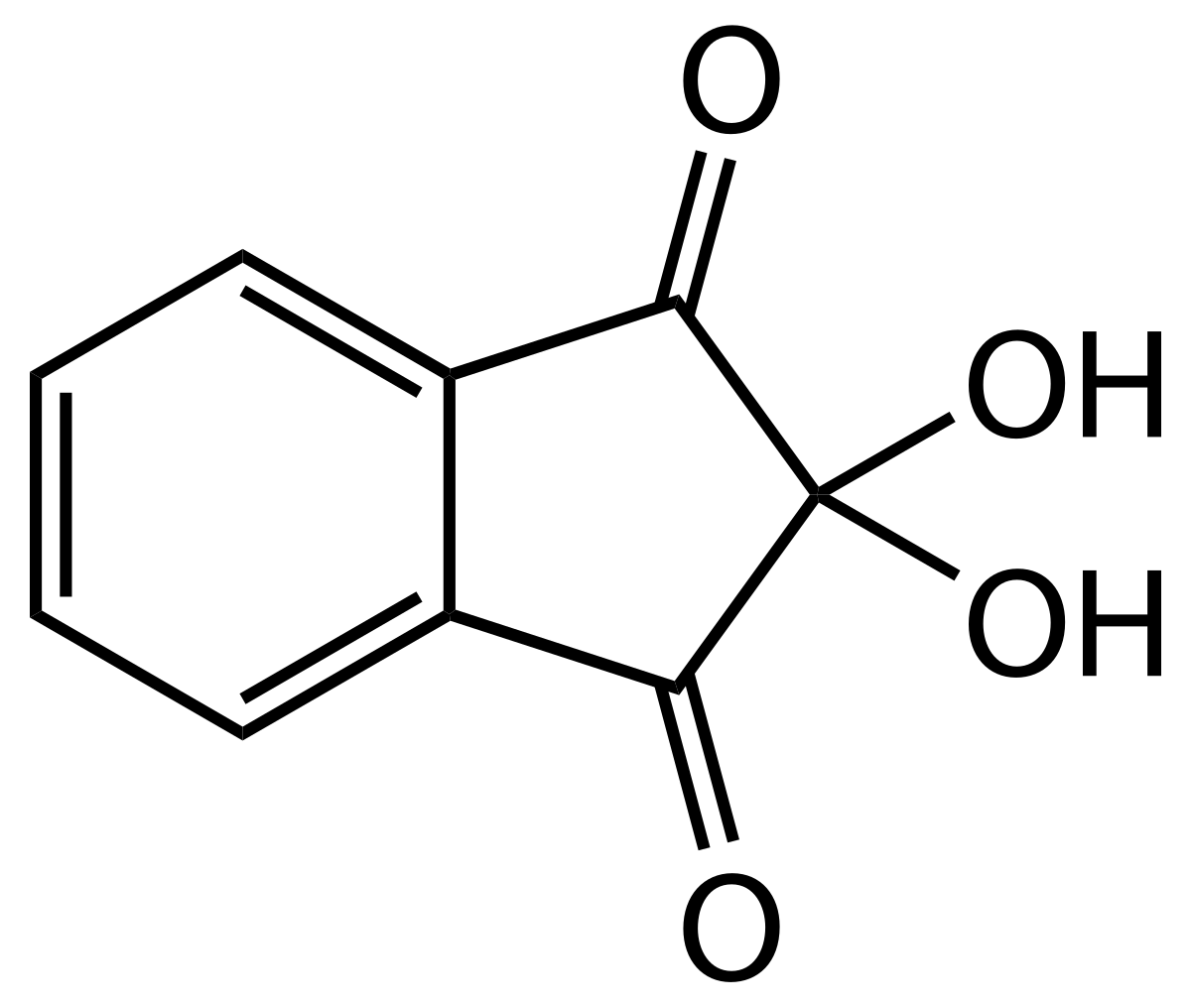


ニンヒドリン Wikipedia
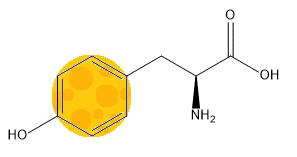


語源で覚える タンパク質の検出反応 化合物語源たん Note



ニンヒドリン反応の利用法と反応機構



化学 ビウレット反応を3分で覚える動画 Youtube



0 件のコメント:
コメントを投稿